近日,四川汇宇制药股份有限公司的“注射用盐酸吉西他滨”(化学药品4类)经国家药品监督管理局公告,批准上市,视同通过一致性评价,获批的规格为:0.2g、1.0g。
吉西他滨是一种核苷同系物,属细胞周期特异性抗肿瘤药,主要杀伤处于S期(DNA合成)的细胞,同时也阻断细胞增殖由G1向S期过渡的进程。本品可用于治疗以下疾病:
- 局部晚期或已转移的非小细胞肺癌;- 本品联合信迪利单抗和铂类化疗适用于不可手术切除的局部晚期或转移性鳞状非小细胞肺癌的一线治疗;- 局部晚期或已转移的胰腺癌;- 吉西他滨与紫杉醇联合,可用于治疗经辅助/新辅助化疗后复发,不能切除的、局部复发或转移性乳腺癌。除非临床上有禁忌,否则既往化疗中应使用过蒽环类抗生素。
吉西他滨可被核苷激酶代谢为二磷酸核苷(dFdCDP)和三磷酸核苷(dFdCTP)。dFdCDP抑制核苷酸还原酶(负责催化生成DNA合成所必需的三磷酸脱氧核苷),导致包括dCTP在内的脱氧核苷浓度降低。dFdCTP与dCTP竞争掺入至DNA 链中。dFdCDP引发的细胞内dCTP浓度降低更加有利于dFdCTP掺入至DNA链中(自增强作用)。吉西他滨核苷掺入至DNA链之后,延伸的DNA链中只增加一个额外的核苷酸,最终导致凋亡性细胞死亡的启动。
吉西他滨是重磅级抗癌药物,于1996年在美国上市,1999年12月在中国上市,先后在全球90多个国家获准上市。吉西他滨亦是广谱抗肿瘤药物,被权威指南(NCCN、CSCO等)推荐用于非小细胞肺癌、胰腺癌、膀胱癌、乳腺癌及其他实体肿瘤的治疗。
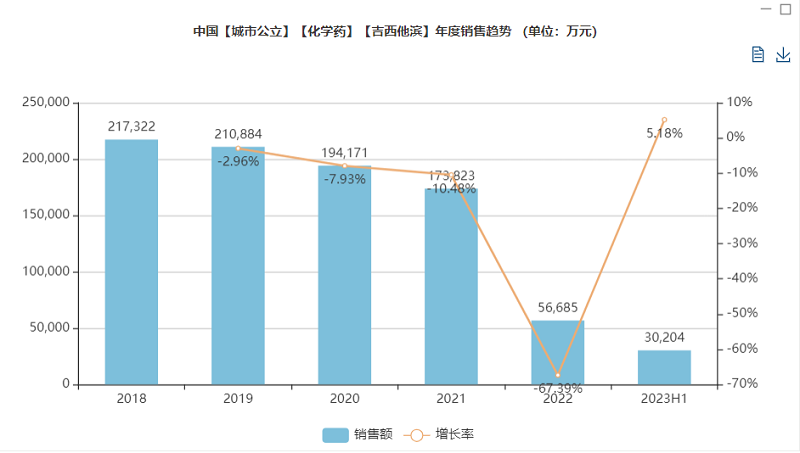
数据来源:米内网
根据米内网数据显示,2022年中国城市公立医院终端注射用盐酸吉西他滨销售额超过 5.6 亿元,2023 年H1中国城市公立医院终端注射用盐酸吉西他滨销售额已达到 3 亿元,同比增速 5.18%。
汇宇研发的注射用盐酸吉西他滨通过仿制药一致性评价,提升了自身的竞争能力,有利于上市销售后取得更大的市场份额。
汇宇制药坚定“为全球患者提供疗效确切、质量精湛、价格合理的药品,让癌症成为一种可以控制的疾病”的使命,目前公司已有 22个药品获批上市,均视同通过注射剂一致性评价,且其中多个品种为首家或前三家过评。未来三年,汇宇制药预期新增超过20个品种获批上市。此外,公司亦在加码创新药研发,全力打造可持续发展的产品矩阵。